
- Tác giả Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:42.
- Sửa đổi lần cuối 2025-01-22 17:13.
Các entanpi tiêu chuẩn của phản ứng (ΔHorxn) có thể tính toán từ tổng của entanpi tiêu chuẩn của sự hình thành của các sản phẩm (mỗi sản phẩm được nhân với hệ số góc của nó) trừ đi tổng của entanpi tiêu chuẩn của sự hình thành của các chất phản ứng (mỗi chất được nhân với hệ số cân bằng của nó) -sản phẩm “
Tương tự như vậy, entanpi tiêu chuẩn của quá trình đốt cháy là gì?
Entanpi tiêu chuẩn của quá trình đốt cháy được định nghĩa là enthalpy thay đổi khi một mol hợp chất được đốt cháy hoàn toàn trong oxi với tất cả các chất phản ứng và sản phẩm của chúng Tiêu chuẩn tiểu bang dưới Tiêu chuẩn điều kiện (298K và áp suất 1 bar).
Cũng biết, đơn vị của entanpi là gì? Các Đơn vị SI đối với entanpi cụ thể là jun trên kilogam. Nó có thể được biểu thị bằng các đại lượng cụ thể khác bằng h = u + pv, trong đó u là nội năng riêng, p là áp suất và v là thể tích riêng, bằng 1ρ, trong đó ρ là khối lượng riêng.
Người ta cũng có thể hỏi, bạn định nghĩa entanpi như thế nào?
Enthalpy là một tính chất nhiệt động lực học của một hệ thống. Nó là tổng của nội năng được cộng vào tích của áp suất và thể tích của hệ. Nó phản ánh khả năng thực hiện công việc phi cơ học và khả năng tỏa nhiệt. Enthalpy được ký hiệu là H; riêng enthalpy ký hiệu là h.
Entanpi của h2o là gì?
enthalpy hình thành cho H2O (l) (- 285,8kJ / mol) nhỏ hơn so với H2O (g) (- 241,82kJ / mol).
Đề xuất:
Entanpi chuẩn của sự hình thành đối với lưu huỳnh đioxit là gì?

Để kiểm tra, nó phải là (&trừ; 296,81 ± 0,20) kJ / mol. Bạn nên sử dụng NIST thường xuyên hơn. Tôi thực sự nhận được &trừ; 310,17 kJ / mol. Trước tiên, bạn phải tra cứu Δ H∘f cho SO3 (g)
Làm thế nào để bạn cân bằng một phương trình đốt cháy?

Cân bằng các phản ứng cháy rất dễ dàng. Đầu tiên, cân bằng nguyên tử cacbon và nguyên tử hydro ở cả hai vế của phương trình. Sau đó, cân bằng các nguyên tử oxy. Cuối cùng, cân bằng bất cứ thứ gì đã trở nên không cân bằng
Làm thế nào để bạn tìm thấy thể tích của một hình lập phương có một hình chóp ở trên?
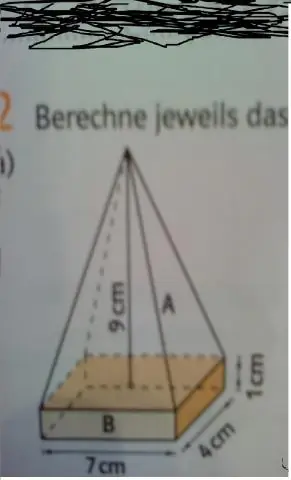
Để tìm thể tích của hình lập phương này, hãy nhân cơ sở với chiều rộng với chiều cao. Để tìm thể tích của hình chóp, hãy lấy diện tích của đáy, egin {align *} Bend {align *} và nhân nó với chiều cao rồi nhân với egin {align *} frac {1} {3} end { căn chỉnh*}
Vật chất di truyền trong mỗi tế bào mới được hình thành qua quá trình phân bào so với vật chất di truyền trong tế bào ban đầu như thế nào?

Nguyên phân tạo ra hai hạt nhân giống hệt hạt nhân ban đầu. Vì vậy, hai tế bào mới được hình thành sau khi phân bào có cùng vật chất di truyền. Trong quá trình nguyên phân, các nhiễm sắc thể ngưng tụ từ chất nhiễm sắc. Khi quan sát bằng kính hiển vi, các nhiễm sắc thể có thể nhìn thấy bên trong nhân sau đó
Làm thế nào để bạn tìm thấy thể tích của một hình nón bên trong một hình trụ?

Công thức cho thể tích của một hình trụ là v = π r2h. Thể tích của hình nón có bán kính là R và chiều cao là H là V = 1/3 π R2H
