
- Tác giả Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:42.
- Sửa đổi lần cuối 2025-01-22 17:13.
Đang giảm dần Sức ép
Sự kết hợp khí ga luật tuyên bố rằng sức ép của một khí ga có liên quan nghịch với âm lượng và liên quan trực tiếp đến nhiệt độ. Nếu giữ nhiệt độ không đổi, phương trình được rút gọn thành định luật Boyle. Do đó, nếu bạn giảm áp suất của một lượng cố định khí ga , nó là âm lượng sẽ tăng.
Ở đây, khi một áp suất được đặt vào một chất khí, thể tích của nó sẽ giảm, do đó chất khí được cho là?
Khi nào âm lượng giảm , áp lực tăng. Điêu nay cho thây răng áp lực của một khí là tỷ lệ nghịch với khối lượng của nó . Điều này được hiển thị bởi NS phương trình sau - thường được gọi là định luật Boyle. Nó được đặt theo tên nhà khoa học thế kỷ 17 Robert Boyle.
Hơn nữa, làm thế nào để giảm áp suất của một chất khí? 1 Câu trả lời. Áp suất khí ga được tạo ra bởi sự va chạm giữa các phân tử của khí ga trong bình chứa và va chạm của các phân tử đó với thành bình. Nhiều va chạm hơn, nhiều hơn nữa sức ép . Đang giảm dần số lượng phân tử sẽ giảm số vụ va chạm và do đó giảm bớt NS sức ép.
Làm thế nào để bạn tìm thấy thể tích của một khí áp suất?
Luật được đưa ra bởi những điều sau đây phương trình : PV = nRT, trong đó P = sức ép , V = âm lượng , n = số mol, R là phổ khí ga hằng số, bằng 0,0821 L-atm / mol-K và T là nhiệt độ tính bằng Kelvin.
Áp suất và thể tích của một chất khí có quan hệ như thế nào?
Hoặc định luật Boyle là một khí ga luật, nêu rõ rằng áp suất và thể tích của một chất khí có mối quan hệ nghịch đảo, khi nhiệt độ được giữ không đổi. Nếu như âm lượng tăng, sau đó sức ép giảm và ngược lại, khi nhiệt độ được giữ không đổi.
Đề xuất:
Mối quan hệ thay đổi giữa thể tích và diện tích bề mặt khi một vật lớn dần lên là gì?
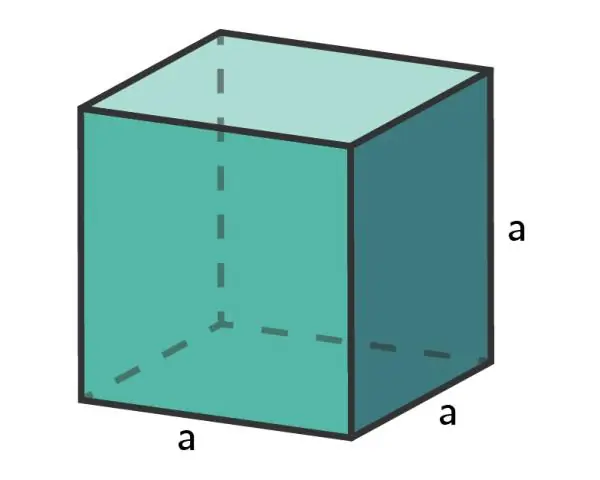
Khi kích thước khối lập phương tăng lên hoặc tế bào lớn hơn, thì tỷ lệ diện tích bề mặt trên thể tích - tỷ lệ SA: V giảm. Khi một đối tượng / ô rất nhỏ, nó có tỷ lệ diện tích bề mặt trên thể tích lớn, trong khi đối tượng / ô lớn có tỷ lệ diện tích bề mặt trên thể tích nhỏ
Làm thế nào một mô hình có thể giúp tìm ra xác suất của một sự kiện phức hợp?
Định nghĩa về xác suất của các sự kiện phức hợp Một sự kiện tổng hợp là một sự kiện trong đó có nhiều hơn một kết quả có thể xảy ra. Việc xác định xác suất của một sự kiện phức hợp bao gồm việc tìm tổng các xác suất của các sự kiện riêng lẻ và nếu cần, loại bỏ bất kỳ xác suất trùng lặp nào
Thể tích của các chất khí có quan hệ như thế nào với nhiệt độ và áp suất của nó?

Thể tích của một lượng khí xác định tỉ lệ nghịch với áp suất của nó khi nhiệt độ không đổi (định luật Boyle). Trong cùng điều kiện nhiệt độ và áp suất, các thể tích bằng nhau của tất cả các chất khí chứa cùng một số phân tử (định luật Avogadro)
Xác suất để một người phụ nữ mù màu kết hôn với một người đàn ông có thị lực bình thường sẽ sinh ra một đứa con mù màu là bao nhiêu?

Nếu một người phụ nữ mang gen bệnh có thị lực bình thường (dị hợp tử về mù màu) kết hôn với một người đàn ông bình thường (XY), thì ở thế hệ F2 có thể có các thế hệ con cháu sau đây: trong số các con gái, 50% là bình thường và 50% là người mang bệnh; trong số con trai, 50% mù màu và 50% thị lực bình thường
Làm thế nào để bạn tìm thấy diện tích bề mặt và thể tích của một hình tròn?

Diện tích bề mặt = (2 • π • r²) + (2 • π • r • chiều cao) Trong đó (2 • π • r²) là diện tích bề mặt của 'đầu mút' và (2 • π • r • chiều cao ) là khu vực bên (khu vực của 'bên')
