
- Tác giả Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:42.
- Sửa đổi lần cuối 2025-01-22 17:13.
Để khắc phục sự cố ổn định, Bohr sửa đổi Mô hình Rutherford bằng cách yêu cầu các electron chuyển động theo quỹ đạo có kích thước và năng lượng cố định. Năng lượng của electron phụ thuộc vào kích thước của quỹ đạo và thấp hơn đối với quỹ đạo nhỏ hơn. Sự phóng xạ chỉ có thể xảy ra khi electron nhảy từ quỹ đạo này sang quỹ đạo khác.
Ngoài ra, mô hình của Bohr khác với Rutherford như thế nào?
Rutherford đã mô tả nguyên tử bao gồm một khối lượng dương cực nhỏ được bao quanh bởi một đám mây electron âm. Bohr cho rằng các electron quay quanh hạt nhân theo các quỹ đạo lượng tử. Bohr được xây dựng dựa trên Mô hình của Rutherford của nguyên tử. Vì vậy, không thể cho các electron chỉ chiếm bất kỳ mức năng lượng nào.
Bohr đã tìm ra những vấn đề gì với lý thuyết của Rutherford? Bohr đã vượt qua vấn đề với Của Rutherford Mô hình nguyên tử bằng cách đề xuất rằng các electron "nhảy" giữa các quỹ đạo khi chúng tăng hoặc mất năng lượng. Do đó, chúng không tồn tại ở trạng thái nằm giữa các quỹ đạo. Các electron mang điện tích âm quay quanh một hạt nhân mang điện tích dương theo những quỹ đạo có mức năng lượng xác định.
Như vậy, Bohr đã sửa đổi mô hình nguyên tử của Rutherford trong hệ mặt trời của Rutherford như thế nào Những hạn chế của mô hình Bohr là gì?
Bohr cải thiện Mô hình nguyên tử của Rutherford bằng cách đề xuất rằng các electron chuyển động theo quỹ đạo tròn với các mức năng lượng cụ thể. Giải trình: Rutherford đề xuất rằng các electron quay quanh hạt nhân giống như các hành tinh xung quanh mặt trời. Khi một kim loại nguyên tử được đốt nóng, nó hấp thụ năng lượng và các electron nhảy lên mức năng lượng cao hơn.
Bohr đã thực hiện những thay đổi nào để nâng cao hiểu biết của chúng ta về nguyên tử?
Năm 1913, Niels Bohr đề xuất một lý thuyết cho hydro nguyên tử dựa trên lý thuyết lượng tử rằng năng lượng chỉ được truyền với một số lượng xác định rõ ràng. Các electron nên chuyển động xung quanh hạt nhân nhưng chỉ theo những quỹ đạo quy định. Khi nhảy từ quỹ đạo này sang quỹ đạo khác có năng lượng thấp hơn, một lượng tử ánh sáng được phát ra.
Đề xuất:
Tại sao Bohr lại sửa đổi mô hình nguyên tử của Rutherford?

Mô hình nguyên tử Bohr: Năm 1913, Bohr đề xuất mô hình lớp vỏ lượng tử hóa của nguyên tử để giải thích cách các electron có thể có quỹ đạo ổn định xung quanh hạt nhân. Để khắc phục vấn đề ổn định, Bohr đã sửa đổi mô hình Rutherford bằng cách yêu cầu các electron chuyển động theo quỹ đạo có kích thước và năng lượng cố định
Tại sao mô hình của Bohr có thể được gọi là mô hình hành tinh của nguyên tử?

Lý do mà nó được gọi là 'mô hình hành tinh' là các electron chuyển động xung quanh hạt nhân giống như các hành tinh chuyển động xung quanh mặt trời (ngoại trừ việc các hành tinh được giữ gần mặt trời bởi lực hấp dẫn, trong khi các electron được giữ gần hạt nhân bởi một thứ gọi là một lực lượng Coulomb)
Làm thế nào mà thí nghiệm của Rutherford bác bỏ mô hình nguyên tử của Thomson?

Ông cho rằng mô hình bánh pudding mận là không chính xác. Sự phân bố điện tích đối xứng sẽ cho phép tất cả các hạt α đi qua mà không bị lệch. Rutherford đề xuất rằng nguyên tử chủ yếu là không gian trống. Các electron quay theo quỹ đạo tròn về một điện tích dương lớn ở tâm
Làm thế nào để bạn tìm thấy thể tích của một hình lập phương có một hình chóp ở trên?
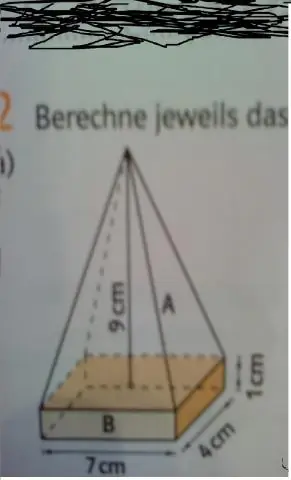
Để tìm thể tích của hình lập phương này, hãy nhân cơ sở với chiều rộng với chiều cao. Để tìm thể tích của hình chóp, hãy lấy diện tích của đáy, egin {align *} Bend {align *} và nhân nó với chiều cao rồi nhân với egin {align *} frac {1} {3} end { căn chỉnh*}
Làm thế nào để bạn tìm thấy thể tích của một hình nón bên trong một hình trụ?

Công thức cho thể tích của một hình trụ là v = π r2h. Thể tích của hình nón có bán kính là R và chiều cao là H là V = 1/3 π R2H
